Introducción
La elección del tratamiento depende del diagnóstico de cada paciente y del estadio de la enfermedad. Un equipo multidisciplinar compuesto por especialistas en oncología, neumología, cirugía, radiología, anatomopatología y radioterapia decidirán el protocolo más indicado para cada caso. Así, se establecerá la realización de cirugía, radioterapia, quimioterapia, inmunoterapia o terapias dirigidas en función de las necesidades del paciente.
Cabe destacar que no todas las personas pacientes recibirán los mismos tratamientos ni todas reaccionarán o evolucionarán de la misma forma a un tratamiento en concreto.
Elección del tratamiento
Elección del tratamiento

Se procederá a elegir un tratamiento oncológico frente al cáncer de pulmón y sus posibilidades de aplicación después, no solo de haberlo diagnosticado, sino de conocer las características de cada caso concreto:
- el tipo de cáncer;
- su tamaño, ubicación y si hay metástasis;
- la edad, estado de salud general y cualquier afección de la persona paciente;
- el grado de afectación de los efectos secundarios de cada tratamiento por parte de la persona paciente;
- y tratamientos oncológicos previos.
En función de estas características del cáncer de pulmón, la persona afectada podrá pasar por uno de los tratamientos descritos más abajo o por la combinación de varios de ellos, bien sea de manera progresiva o simultánea.
Es posible que, durante el proceso de tratamiento, las características del tumor cambien o se encuentren nuevos nódulos que indiquen metástasis en el propio pulmón o en otras partes del cuerpo.
También puede darse que el tratamiento aplicado afecte a otros órganos sanos, que la toxicidad de los fármacos altere algunas funciones vitales o que los efectos adversos afecten sobremanera a la calidad de vida de la persona paciente.
Por ello, a lo largo de todo este proceso, se efectúa un seguimiento de la persona paciente, de su cáncer y de su respuesta al tratamiento que se está aplicando. El equipo médico puede considerar variar el tratamiento en función de los cambios encontrados en el seguimiento.
Tipos de tratamientos
Tipos de tratamientos
CIRUGÍA
Cirugía
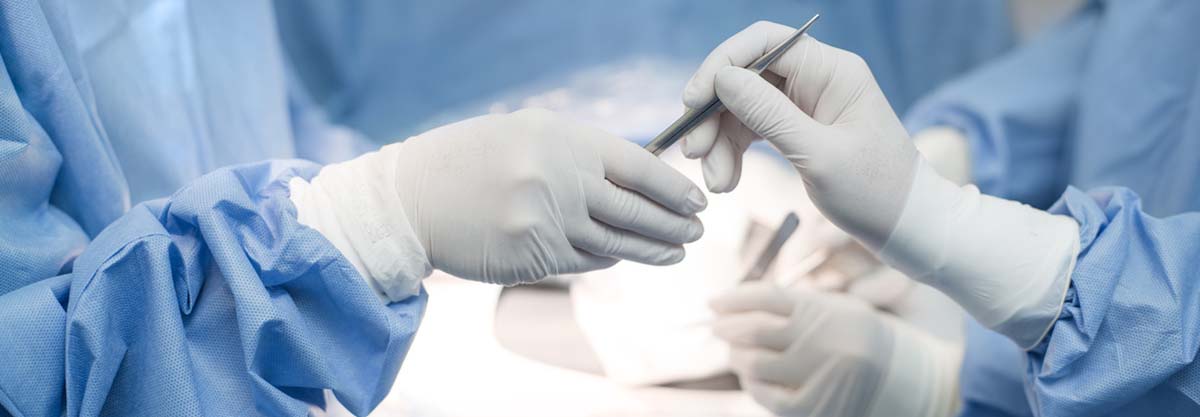
Es la opción habitual para las personas con un estado de salud general bueno y cuyo cáncer de pulmón se encuentra localizado (sin metástasis) y en etapa temprana. Esta práctica consiste en extirpar completamente todas las células tumorales. El tamaño y ubicación del tumor determinarán el tipo de cirugía a practicar.
- Lobectomía. Cuando el cáncer está localizado en uno de los lóbulos de un pulmón tres en el derecho y dos en el izquierdo–, se extirpa la totalidad del lóbulo en el que se aloja y los ganglios linfáticos en el hilio y mediastino asociado a él.
- Resección sublobar. En caso de que el tumor tenga un tamaño muy reducido o que las funciones pulmonares no permitan la extirpación de todo un lóbulo, puede aplicarse esta cirugía consistente en la extirpación del fragmento del lóbulo pulmonar en el que se encuentra el tumor.
- Resección en cuña o resección sublobar no-anatómica. Se realiza en las personas pacientes demasiado enfermas para la lobectomía, para los pequeños tumores que se localizan periféricamente y los límites anatómicos cruzados, o con tumores primarios múltiples de NSCLC.
- Segmentectomía o resección segmentaria. Del mismo modo que los pulmones se dividen en lóbulos, estos, a su vez, se dividen en segmentos funcionales. En esta cirugía se extirpa la totalidad del segmento en el que se aloja el cáncer.
- Pneumonectomía. Consiste en la extracción del pulmón entero afectado por el cáncer. Se lleva a cabo en los casos en los que el tumor ha alcanzado un tamaño considerable, se encuentra cerca de la arteria o vena pulmonar principales o de los bronquios. Su aplicación no es recomendada en pacientes de avanzada edad o que sufran un deterioro de las funciones pulmonares.
- Mediastinoscopia. Es un procedimiento para examinar los órganos ubicados en el área entre los pulmones y obtener una muestra de los ganglios linfáticos cercanos.
Se lleva a cabo siempre que se considere que el resto de las funciones pulmonares pueden seguir inalterables sin perjudicar a la calidad de vida de la persona paciente.
Comparada con la lobectomía, la resección sublobar conlleva una inferior pérdida de las funciones pulmonares pero, debido al peligro existente de que las células cancerosas estén diseminadas por un área mayor, puede que posteriormente se requiera la extirpación del lóbulo en su totalidad.
Normalmente se aplica en casos de tumores que se encuentran en lo profundo del lóbulo medio del pulmón derecho.
Esta práctica es apta en casos de adenocarcinoma (especialmente el subtipo lepídico) de tamaño inferior a 2 cm y que no haya afectado a los ganglios linfáticos. Es un procedimiento más complejo que requiere un amplio conocimiento de la anatomía pulmonar.
Se lleva a cabo con la ayuda de un mediastinoscopio con una luz y una lente para observar. Con él se puede extraer tejido para su análisis con el fin de verificar si hay signos de enfermedad. Se realiza mediante una incisión por encima del esternón.
Para más información puedes ver este vídeo de Medtronic
QUIMIOTERAPIA
Quimioterapia

La quimioterapia son fármacos que ralentizan el crecimiento y reproducción de todas las células en general, pero en especial, las cancerosas. Esto puede significar la reducción del tumor e, incluso en ocasiones, hacerlo desaparecer por completo.
El tratamiento de quimioterapia puede estar compuesto por uno o varios fármacos y puede sufrir variaciones a lo largo del proceso de la enfermedad dependiendo de si el tumor responde de manera favorable o no a cada una de las sesiones.
A diferencia de los cánceres de pulmón no microcítico, para los cuales se han investigado y desarrollado diferentes tipos de terapias, en casos de cáncer de pulmón de células pequeñas en los que está limitado a tórax, la combinación de quimioterapia y radioterapia torácica es fundamental.
La aplicación de estos fármacos puede ser de diferentes tipos.
- Neoadyuvante, como paso previo a una cirugía o radioterapia para reducir el tamaño de los tumores.
- Adyuvante, como complemento a tratamientos de cirugía o radioterapia localizados para asegurar que no queda rastro de cualquier célula cancerosa.
- Como terapia frente a un cáncer recurrente que vuelve a aparecer.
- Como terapia frente a un cáncer metastásico diseminado por otras partes del cuerpo.
La quimioterapia puede administrarse de varias siguientes maneras.
- Vía oral. Son fármacos en forma de pastillas, comprimidos, cápsulas o líquidos. Los medicamentos que se administran por esta vía son aquellos que permiten una rápida absorción sublingual o porque los ácidos gástricos no los destruyen.
- Vía intravenosa (IV).Es la forma más habitual de aplicación. Los fármacos se inyectan directamente en vena, lo que permite su inclusión directa en el torrente sanguíneo.
- Mediante angiocatéter en una vena de la mano o el brazo. Es un utensilio temporal que cuyo uso puede durar desde unos minutos a unos pocos días.
- Mediante vía PICC, empleada en infusiones cortas o si se necesita que la aplicación del fármaco sea continua. El uso de estas vías puede durar entre seis semanas y unos pocos meses.
- Mediante catéteres no tunelizados aplicados directamente en la vena yugular o subclavia para dirigir los fármacos directamente al corazón.
- Mediante catéteres tunelizados aplicados de manera subcutánea en el pecho de la persona paciente y que dirigen el fármaco directamente al corazón.
- Mediante Port-a-Cath cuando el caso requiere de una aplicación permanente. Este instrumento se instala bajo la piel del pecho de la persona paciente mediante una intervención radiológica o quirúrgica. Está provisto de un catéter que, como los anteriores, dirige el medicamento al corazón.
- Quimioterapia intrapleural. Utilizada normalmente para aliviar la dificultad de respiración y otros síntomas derivados de la acumulación de líquido pleural maligno.
Además, en este último caso, los medicamentos deben ser fácilmente absorbibles a través de las paredes del estómago o del intestino. Algunos fármacos que pueden administrarse de forma oral también se pueden encontrar para administraciones intravenosas dependiendo de su fuerza o cantidad necesaria.
El proceso puede durar minutos u horas, aunque en ocasiones se necesita que los fármacos se administren durante días o semanas. Para ello se provee a la persona paciente con una bomba portátil que permite la administración del medicamento sin interrupciones, tanto en el hospital como en domicilio.
Las formas de aplicación en cáncer de pulmón pueden ser:
Este método implica el uso de un catéter más largo aplicado en una vena más grande del brazo. Debe confirmarse que el catéter está en el lugar adecuado mediante una fluoroscopia con rayos X..
Su uso está recomendado en aplicaciones a corto plazo o de emergencia por riesgo de infecciones. De nuevo se debe realizar una fluoroscopia para confirmar su correcta instalación e implican un mantenimiento continuo y cambios de vendaje.
Se necesita formar tejido cicatricial alrededor de un manguito dracón para la posición del catéter y, al igual que las técnicas anteriores, requiere una fluoroscopia que confirme su correcta colocación. Al contrario que el método anterior, este catéter puede utilizarse durante años con una baja probabilidad de causar infecciones. Pueden tener entre una y tres entradas (lúmenes) utilizadas tanto para la infusión de fármacos como para la extracción de sangre.
Permite llevar una bomba de infusión continua que evita la hospitalización de la persona paciente. Requiere de cierto mantenimiento aunque no cambios de vendaje.
Mediante esta técnica, se drena el líquido canceroso para luego administrar los fármacos directamente entre el pulmón y la pleura.
Debido a que la quimioterapia afecta a la totalidad de las células del cuerpo –cancerosas o no– se producen efectos secundarios debido a anomalías en otras funciones vitales u órganos de la persona paciente. Entre los más frecuentes hay que mencionar:
- caída del cabello;
- úlceras en la boca;
- pérdida de apetito o cambios en el peso;
- náuseas y vómitos;
- y diarrea o estreñimiento.
Otros efectos secundarios derivados de la afectación de células de la médula ósea producen componentes sanguíneos pueden causar:
- aumento de la probabilidad de infecciones en caso de disminución de glóbulos blancos;
- tendencia a sangrados y moratones en caso de disminución de las plaquetas;
- y cansancio en caso de disminución de glóbulos rojos.
Para minimizar estos efectos, la aplicación de este tratamiento tiene unas pausas temporales. Por regla general, la aplicación del tratamiento se lleva a cabo en sesiones distanciadas temporalmente de unas tres semanas. De esta manera se consigue la regeneración de las células sanas y, con ella, la recuperación de la persona paciente para poder afrontar una nueva sesión. A este periodo entre dos sesiones se lo conoce como ciclo.
En ocasiones, los ciclos son inferior a estas tres semanas. Esto se hace con el objetivo de que la inmunoterapia sea más eficaz contra algunos tipos de cáncer, pero, a su vez, también implica mayor riesgo de padecer efectos secundarios.
La sucesión de ciclos –conocida a su vez como curso de quimioterapia– suele tener una duración establecida, aunque, en ocasiones, la persona paciente recibe el tratamiento de quimioterapia mientras esta funcione, siempre que los efectos secundarios lo permitan.
RADIOTERAPIA
Radioterapia
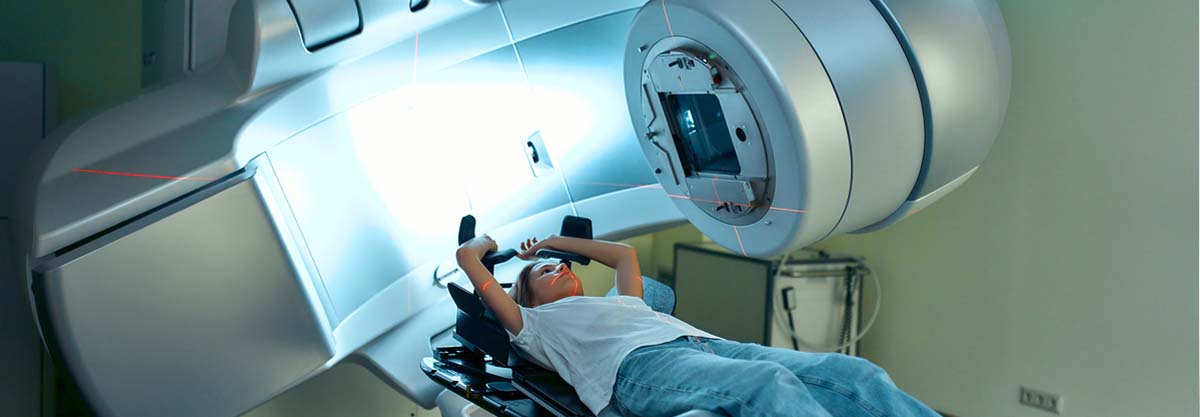
La radioterapia es la aplicación de radiación de rayos X de alta energía que puede destruir células cancerosas. Al igual que la quimioterapia, su empleo puede utilizarse de variadas formas.
- Primaria. Como único tratamiento con el objetivo de eliminar el tumor. Esto sucede cuando éste se encuentra localizado, cuando responde favorablemente a los fármacos y en los casos en los que la cirugía y/o quimioterapia no aseguran una mayor supervivencia de la persona paciente (como en casos de carcinoma microcítico).
- Neoadyuvante. Como paso previo a una cirugía o radioterapia para reducir el tamaño de los tumores.
- Adyuvante. Como complemento a tratamientos de cirugía o quimioterapia localizados para asegurar que no queda rastro de cualquier célula cancerosa
- Como terapia frente a un cáncer recurrente que vuelve a aparecer.
- Como terapia frente a un cáncer metastásico diseminado por otras partes del cuerpo.
- Para paliar los síntomas de la enfermedad.
Existen dos tipos principales de radioterapia: de haz externo y braquiterapia.
- Haz externo. Se aplican los rayos X desde fuera del cuerpo directamente al tumor, lo que disminuye la exposición a la radiación del tejido sano circundante.
- Radioterapia estereotáctica del cuerpo (SBRT). Se aplica a tumores diseminados a otros órganos o a aquellas personas que no pueden tratarse con cirugía por su edad avanzada, por sufrir insuficiencia cardíaca crónica o por tomar medicamentos diluyentes de la sangre que suponen un peligro de hemorragia.
- Radioterapia conformada en 3D (3D-CRT). Es un método asistido por computadoras sofisticadas que determinan de forma precisa la posición de uno o varios tumores que posteriormente se radiarán desde diferentes direcciones.
- Radioterapia de intensidad modulada (IMRP). Es una terapia tridimensional en la que la intensidad de cada uno de los rayos puede ajustarse para evitar daños en los tejidos sanos. Esta técnica se utiliza sobre todo en casos en los que el tumor está cerca de estructuras importantes como la médula espinal.
- Terapia de arco modulado (VMAT). Es una variante del anterior en la que la máquina de radiación rota alrededor del cuerpo durante el tratamiento. Esto reduce el tiempo de la sesión a unos pocos minutos.
- Radiocirugía estereotáctica (SRS). Pese a su nombre, no es una cirugía sino un tipo de radioterapia estereotáctica que se administra, por lo general, en una única sesión que dura desde minutos a horas.
- Braquiterapia. Se utiliza con el fin de aliviar los síntomas del cáncer reduciendo el tamaño de tumores que se encuentran obstruyendo las vías respiratorias o en zonas circundantes a un tumor que se ha extraído mediante cirugía previa.
Tiene el objetivo de tratar el cáncer de pulmón y su propagación a otros órganos. Es un método similar a la realización de una radiografía con la diferencia de poseer una dosis de radiación más elevada.
Cada sesión dura unos minutos y, dependiendo del caso oncológico, pueden llegar a administrarse tratamientos durante varios días a la semana y a lo largo de varias semanas. Algunas técnicas son:
La/el paciente se coloca en un armazón adecuado para su tratamiento y se radia el tumor con múltiples haces de rayos desde diferentes direcciones. Debido a su alta dosis de radiación no son necesarios tratamientos tan prolongados en el tiempo.
Este método requiere una operación quirúrgica en la que se aplican unas partículas o semillas de material radiactivo directamente sobre el tumor o en la vía respiratoria en la que este se aloja (normalmente en los bronquios).
La radiación tiene un corto recorrido desde las semillas, minimizando la exposición de tejido sano. Lo más común es retirar dichas partículas transcurrido un tiempo aunque, en ocasiones, puede quedar permanentemente en la zona, disminuyendo su carga radioactiva con el transcurso del tiempo.
Aunque esta terapia se basa en infundir una determinada dosis de radiación al tumor y a los tejidos circundantes, pueden aparecer efectos secundarios más allá de la zona donde se localiza el tumor. Normalmente, estos efectos suelen mitigar o incluso desaparecer al haber finalizado el tratamiento. Algunos de ellos pueden ser más fuertes si la radioterapia se combina con alguna otra terapia. Los efectos más comunes son:
- pérdida de pelo en la zona donde se radia;
- cansancio;
- náuseas y/o vómitos;
- pérdida de apetito o cambios en el peso;
- y alteraciones de la piel en el área tratada. Puede producirse un enrojecimiento de la piel, aparición de ampollas o incluso descamación.
En el caso de pacientes de cáncer de pulmón, la zona en la que se aplica esta radiación suele ser la parte del tórax. Por ello, los órganos a los que van dirigidos los rayos X –en este caso pulmones y esófago– pueden resultar dañados. Ello se puede traducir en:
- problemas respiratorios;
- necesidad de hacer respiraciones cortas;
- dolor de garganta;
- dificultad para tragar.
En aquellos casos en los que el tumor se haya esparcido y haya llegado al cerebro, puede necesitarse la aplicación de la radioterapia en esta zona. Esta práctica puede conllevar:
- pérdida de memoria;
- dolor de cabeza;
- y dificultad para pensar o concentrarse.
INMUNOTERAPIA
Inmunoterapia
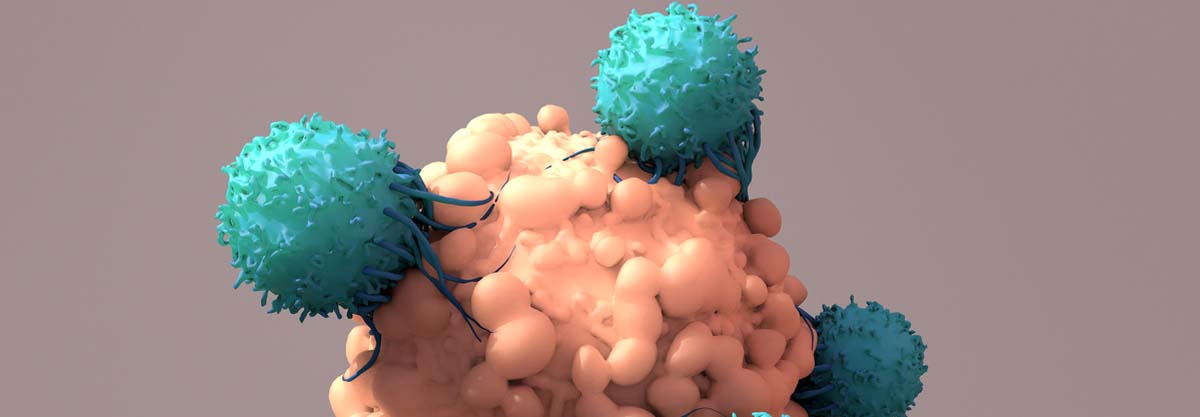
El sistema inmunitario del cuerpo está preparado para combatir las células y microorganismos malignos. Algunas células, como los linfocitos T, están programadas para reconocer y responder frente a estos microorganismos e incluso para recordar a aquellos contra los que ya se han enfrentado en el pasado.
Ante la presencia de células malignas, los linfocitos T acuden a destruirlas o alertan a otras células para combatirlas. En el caso del cáncer, las células malignas están provistas en su superficie por unas proteínas –como la PD-1, la PD-L1 o la CTLA-4– que bloquean los receptores de la superficie de los linfocitos T. Esto significa que los linfocitos no reaccionan ante el tumor como sí lo hacen frente a otras células malignas.
La inmunoterapia, a diferencia del resto de las terapias, no está dirigida a terminar con el tumor, sino que pretende estimular el sistema inmunitario de la propia persona paciente para que reconozca las células tumorales como malignas.
Además, con ella se consigue que el sistema inmunitario ataque solo a aquellas células cancerígenas, dejando a las células sanas intactas, reduciendo así la toxicidad de los fármacos. Otra de las ventajas de la inmunoterapia es que consigue que los linfocitos T sigan reconociendo el tumor como maligno, manteniendo así una respuesta inmunitaria ante él e incrementando las posibilidades de una supervivencia más prolongada.
Por lo tanto, la inmunoterapia consta de fármacos con sustancias producidas por el propio cuerpo o sintetizadas en un laboratorio que actúan sobre el cáncer de las siguientes maneras:
- detienen o retrasan el crecimiento de las células tumorales;
- impiden que el cáncer se disemine a otras partes del cuerpo;
- y ayuda al cuerpo a combatir el cáncer por sí mismo.
Esta terapia puede administrarse como tratamiento único o combinada con la quimioterapia para una respuesta terapéutica más efectiva.
Existen diferentes tipos de inmunoterapia:
- Anticuerpos monoclonales. Este método se puede considerar tanto dentro de la inmunoterapia como en las terapias dirigidas. Estos anticuerpos se sintetizan en un laboratorio con el fin de que el sistema inmunitario reconozca una proteína anormal específica de la célula tumoral, ataque a estas células y las elimine.
- Inmunoterapias no específicas. Estas suelen utilizarse junto con quimioterapia o radioterapia, aunque algunas se administran como tratamiento principal.
- Terapia con virus oncolíticos. Es un método en el cual se inyectan en las células cancerosas unos virus modificados genéticamente. Una vez dentro de estas células, el virus se reproduce hasta provocar la explosión de la célula liberando antígenos.
- Terapias con células T o CAR (Chimeric Antigen Receptor, Receptores de Antígenos Quiméricos). Las células T son un tipo de glóbulos blancos creados por nuestro propio sistema inmunológico para combatir infecciones y otras enfermedades.
- Vacunas contra el cáncer. Las vacunas comunes se administran para prevenir de futuras infecciones. Para ello, utilizan gérmenes debilitados o muertos para favorecer una respuesta del sistema inmunitario frente a ellos. En el caso de las vacunas contra el cáncer ocurre lo mismo, pero la respuesta inmunitaria se dirige a células cancerosas. Existen dos tipos de vacunas:
- Vacunas para prevención. Son las que previenen de virus e infecciones que pueden derivar en tumores. Un ejemplo de ello es el cáncer de cuello uterino que en la mayoría de las ocasiones es provocado por una infección por el Virus del Papiloma Humano (VPH).
- Vacunas para tratamiento. Estas vacunas preparan al sistema inmunitario contra enfermedades ya existentes en el organismo, como la presencia de células cancerosas.
En el caso del cáncer de pulmón, no hay ninguna infección que indique una posible aparición del tumor.
En estos casos, las vacunas se componen de dichas células cancerosas, partes de ellas o de antígenos (uno o varios) presentes en ellas.
Para ello, nuevamente, las células inmunitarias de la persona paciente se extraen para exponerlas a estas sustancias en los laboratorios. De esta manera, cuando vuelven a administrarse, el sistema inmunitario aumenta su respuesta contra las células tumorales.
Nuestro sistema inmunitario posee células de memoria, es decir, está preparado para atacar a aquellos virus o infecciones que se han tenido anteriormente. Por ello, se espera que estas vacunas puedan seguir mostrando resultados favorables mucho después de haberse administrado.
Otro tipo de anticuerpos actúan, como se comentaba anteriormente, liberando los frenos del sistema inmunitario ante las proteínas antes mencionadas –también conocidas puntos de control inmunitarios– presentes en la superficie de las células tumorales. De esta manera, se pasa a considerar estas células como malignas y el propio cuerpo interviene en su contra.
Estas terapias constan de unas sustancias (interferones e interleucinas) que tienen como fin la destrucción de las células tumorales. En el caso de las investigaciones con respecto al cáncer de pulmón, debido a la falta de especificidad de los resultados hacen que, actualmente, su uso sea limitado.
El sistema inmunitario ataca a todas las células que tengan estos antígenos, con lo cual, las células sanas no se ven afectadas.
Se extrae sangre del paciente para obtener estas células. En un laboratorio, se modifican con el fin de proveerlas con unas proteínas específicas conocidas como receptores y se vuelven a inyectar en el paciente. Estos receptores permiten a las células T reconocer a las cancerosas y las destruyen.
Pese a todo lo comentado, la inmunoterapia no está exenta de efectos secundarios. Una activación del sistema inmunitario puede hacer que éste afecte a otros órganos que están sanos e incluso puede desarrollar enfermedades autoinmunes hasta el momento desconocidas por las personas pacientes. Otros posibles efectos secundarios de estas terapias pueden ser:
- aumento de peso;
- presión arterial baja;
- síntomas similares a la gripe;
- fatiga.
- fiebre;
- escalofrios;
- náuseas;
- dolor en el lugar de la inyección;
- erupciones cutáneas o picor en la piel;
- diarrea;
- inflamación del hígado o pulmones (tos y dificultad para respirar);
- y alteración hormonal.
No todos estos síntomas aparecen en el mismo momento del tratamiento. Hay algunos que se manifiestan en desde las primeras sesiones, como los problemas cutáneos. Otros, en cambio, aparecen cuando el tratamiento está en fases más avanzadas.
Algunos de los efectos secundarios pueden ser leves o moderados, pero otros pueden resultar importantes e incluso poner en riesgo la vida de la persona paciente. Según la gravedad, puede tener que alterarse o suprimirse el tratamiento. Por ello, cualquiera de los efectos secundarios provocados por la inmunoterapia deben ser trasladados al equipo médico para proceder a su propio tratamiento.
Para más información puedes ver este vídeo de Fundación Más Que Ideas
TERAPIAS DIRIGIDAS
Terapias dirigidas

Los tumores pueden clasificarse en varios tipos y, tambiénse organizan según su mutación (ver información sobre biomarcadores). Estas mutaciones son ‘dianas biológicas’ que permiten a los oncólogos predecir qué tipo de tratamiento será más efectivo en determinado tipo de pacientes.
Estos son fármacos biológicos compuestos por sustancias más específicas y menos tóxicas que la quimioterapia que actúan bloqueando los mecanismos que favorecen el crecimiento y desarrollo celular reduciendo o frenando así el desarrollo tumoral. La elección de los fármacos se realiza en función, no sólo del tipo de mutación, sino también dependiendo del estadio de la enfermedad.
Las personas tratadas con este tipo de medicamentos pueden duplicar su supervivencia mediante una terapia oral, mejorando su supervivencia y calidad de vida en comparación a la quimioterapia tradicional.
Con estos fármacos debe tenerse especial cuidado puesto que, no solo pueden tener interacciones con otros medicamentos (oncológicos o no), sino que puede que su efectividad se vea afectada por productos de comercios como herboristerías o incluso por ciertos alimentos.
- Medicamentos dirigidos al crecimiento de los vasos sanguíneos del tumor (angiogénesis). Los tumores generan sus propios vasos sanguíneos que les proporcionan todo lo que necesitan para seguir creciendo. Esto también les sirve de ayuda para diseminarse por otros órganos del cuerpo.
- hipertensióna;
- fatiga;
- sangrado;
- descenso de niveles de glóbulos blancos (predisposición a infecciones);
- dolores de cabeza;
- úlceras en la boca;
- pérdida del apetito;
- y diarrea.
- coágulos sanguíneos;
- sangrados abundantes;
- perforaciones en intestinos;
- problemas cardíacos;
- y lenta cicatrización de heridas.
Algunos medicamentos de estas terapias son inhibidores de la angiogénesis y actúan evitando la vascularización de los tumores, afectando indirectamente al desarrollo y difusión de estos. Los más utilizados contra el cáncer de pulmón no microcítico avanzado son el bevacizumab y el ramucirumab.
Los efectos secundarios más comunes de esta terapia son:
Otros efectos más graves pero menos comunes son:
Debido a estos efectos secundarios, estas terapias no son aptas para pacientes con sangrado en el esputo o que estén tomando medicamentos anticoagulantes.
- Medicamentos contra células con mutación en gen EGFR. El EGFR es una proteína que interviene en el crecimiento y la división de las células. En ocasiones, células del cáncer de pulmón no microcítico tienen un exceso de esta proteína en su superficie, lo que implica un crecimiento más rápido del tumor.
- Inhibidores del EGFR en cáncer de pulmón no microcítico. Suelen utilizarse como primer tratamiento cuando el cáncer está en fase avanzada, aunque algunos se pueden administrar como adyuvantes a una cirugía en cánceres en etapas iniciales. Otros pueden utilizarse junto con medicamentos contra angiogénesis.
- Inhibidores del EGFR contra células con mutación T790M. Los medicamentos inhibidores de EGFR pueden resultar útiles durante algunos meses en la reducción de tumores. En ocasiones, pasado un tiempo de estar en este tratamiento, este deja de ser efectivo debido a una nueva mutación del gen EGFR conocida como T790M. Cuando el tumor vuelve a progresar cuando se está tomando un tratamiento así, se hace una biopsia para comprobar si se ha dado esta mutación.
- problemas y/o erupciones cutáneas;
- diarrea;
- úlceras en la boca;
- y pérdida de apetito.
Los medicamentos de esta terapia inhiben la señal del EGFR. Esta mutación suele ser común en mujeres, asiáticos y personas no fumadoras.
Los efectos secundarios más comunes de estos medicamentos suelen ser:
Uno de los efectos secundarios más graves pero menos comunes es la bajada de ciertos minerales en sangre, que puede afectar el ritmo cardíaco.
- Medicamentos contra células con reordenamiento en ALK. Este tipo de reordenamiento es común en personas jóvenes, no fumadoras que sufren de adenocarcinoma. El reordenamiento en el gen ALK produce una proteína anormal ALK, esto se traduce en un mayor crecimiento y propagación de las células cancerosas. Se recurre a estos medicamentos cuando el tumor está en fase avanzada y la quimioterapia deja de tener efecto o en sustitución de esta.
- náuseas y vómitos;
- diarrea;
- estreñimiento;
- fatiga;
- y alteración de la visión.
- inflamación de los pulmones u otros órganos;
- daño hepático;
- daño del sistema nervioso;
- y problemas en el ritmo cardíaco.
- Medicamentos contra células con reordenamiento en ROS-1. Este reordenamiento se produce en algunos cánceres de pulmón no microcítico y similar al del ALK, siendo posible que algunos medicamentos ataquen a ambos genes.
- mareos;
- diarrea o estreñimiento;
- fatiga;
- y alteración de la visión.
- inflamación de los pulmones u otros órganos;
- daño hepático;
- daño del sistema nervioso;
- problemas en el ritmo cardíaco.
- Medicamentos contra células con mutación en gen BRAFV600. Se da en cánceres de pulmón no microcítico. Las proteínas alteradas BRAF derivadas del cambio en dicho gen, favorecen el crecimiento del tumor.
- engrosamiento de la piel;
- erupciones cutáneaso;
- picazón;
- ensibilidad al sol;
- dolor de cabeza;
- fiebre;
- dolor de las articulaciones;
- fatiga;
- pérdida del cabello;
- náuseas;
- y diarrea.
- sangrado;
- problemas en el ritmo cardíaco;
- problemas hepáticos o renales;
- problemas en pulmones;
- reacciones alérgicas graves;
- problemas graves en piel y/o ojos;
- subida del nivel de azúcar en sangre;
- y cáncer de piel de células escamosas.
- Medicamentos contra células con reordenamiento en RET. La proteína anormal RET generada por la mutación en este mismo gen ayuda en el crecimiento de las células tumorales.
- sequedad de la boc;
- diarrea o estreñimiento;
- hipertensión;
- fatiga;
- hinchazón en manos y/o pies;
- erupciones en la piel;
- subida del nivel de azúcar en sangre;
- dolor en músculos y/o articulaciones;
- niveles bajos de glóbulos blancos, glóbulos rojos o plaquetas;
- y alteraciones en otros análisis de sangre.
- daño hepático;
- daño en los pulmones;
- reacciones alérgicas;
- problemas en el ritmo cardíaco;
- propensión al sangrado;
- y problemas en la cicatrización de heridas.
- Medicamentos contra células con mutación en gen METexon14. La proteína MET alterada fruto del cambio en este gen favorece el crecimiento y propagación de las células tumorales.
- diarrea o estreñimiento;
- náuseas y/o vómitos;
- fatiga y debilidad;
- pérdida de apetito;
- hinchazón en manos y/o pies;
- y alteraciones en otros análisis de sangre.
- hinchazón o fibrosis en los pulmones;
- daños hepáticos;
- y sensibilidad a la luz solar u otras fuentes de rayos UV.
- Medicamentos contra células con reordenamiento en NTRK. La proteína NTRK alterada de dicho reordenamiento provoca un crecimiento anormal de las células y con ello el cáncer.
- diarrea o estreñimiento;
- náuseas y/o vómitos;
- fatiga y debilidad;
- y aumento de peso.
- aturdimiento o confusión;
- daños hepáticos;
- y problemas cardíacos.
Los efectos secundarios más comunes son:
Otros efectos secundarios más graves pueden ser:
Pueden utilizarse en etapas avanzadas como primer tratamiento en sustitución de la quimioterapia. Algunos también son eficaces en casos de metástasis.
Sus efectos secundarios:
Al igual que los medicamentos contra mutaciones ALK, los de ROS-1 pueden presentar en la persona paciente los siguientes síntomas graves:
Los medicamentos que atacan a las células con esta mutación pueden usarse solos o combinados en casos de metástasis.
Algunos de sus efectos secundarios son:
Otros efectos secundarios más graves aunque menos frecuentes pueden ser:
Los efectos secundarios más comunes de los medicamentos inhibidores de RET son:
Otros efectos secundarios más graves pero menos frecuentes pueden ser:
Los inhibidores de esta proteína se pueden usar para tratar cánceres de pulmón no microcítico con metástasis.
Los efectos secundarios más comunes de los medicamentos inhibidores de MET son:
Otros efectos secundarios más graves pero menos frecuentes pueden ser:
Los inhibidores de esta proteína se emplean en cánceres de pulmón no microcítico avanzados que han crecido siendo tratados con otros medicamentos.
Los efectos secundarios más comunes de los medicamentos inhibidores de NTRK son:
Otros efectos secundarios más graves pero menos frecuentes pueden ser:
Existen otros cuidados relativos a otras áreas y disciplinas que abarcan desde la administración de medicamentos, el uso de la cirugía o el asesoramiento nutricional hasta las técnicas de relajación o el apoyo emocional y el soporte religioso o espiritual.
- Radioterapia. Puede ayudar a reducir la obstrucción de vías respiratorias por el propio tumor o por el sangrado del mismo.
- Broncoscopia. Puede servir para abrir vías respiratorias obstruidas.
- Cirugía. Puede ser útil para abrir vías respiratorias mediante la colocación de una endoprótesis o a reforzar los huesos afectados por metástasis mediante implantes.
- Administración de medicamentos. Pueden ayudar a aliviar los dolores provocados por el tumor y/o la dificultad de respirar, reducir o eliminar la tos, abrir vías respiratorias cerradas, reducir secreciones bronquiales, reducir la inflamación causada por el propio cáncer o por la radioterapia, fortalecer los huesos, reducir el dolor en estos y prevenir las metástasis en ellos.
- Oxigenoterapia. Puede llegar a compensar la poca capacidad de los pulmones afectados por cáncer de pulmón para extraer el oxígeno del aire.
- Terapia nutricional. Los estimulantes del apetito o los suplementos nutricionales pueden favorecer la nutrición de la persona paciente y reducir la pérdida de peso.
- Terapias psicológicas. En ocasiones, el estado de ánimo puede afectar a la calidad de vida y a los efectos de los tratamientos. Las sesiones con profesionales de la psicología especializada en casos oncológicos o el contacto con grupos de pacientes pueden resultar de gran ayuda.
- Asesoramiento laboral.Las preocupaciones sobre bajas laborales o incapacidades suelen aparecer en la época del diagnóstico. En otros casos, este apoyo legal es útil para tramitar la reincorporación al trabajo de las personas supervivientes
- Trabajo social. Puede ser útil en casos de problemas económicos y otras situaciones de desprotección social de la persona paciente y a su familia.
- Terapia religiosa o espiritual. En caso de profesar alguna religión, mantener la práctica puede resultar satisfactorio para la persona paciente.
- Ayuda para afrontar los últimos días. Son el conjunto de acciones que se llevan a cabo en la última etapa en caso de que los tratamientos no hayan funcionado y la enfermedad haya avanzado Se trata de evitar el dolor y atender cualquier necesidad de la persona paciente y de sus familiares para hacer más llevadero este periodo.
Líneas de tratamientos
Líneas de tratamientos
Las personas pacientes de cáncer de pulmón, suelen requerir diferentes tratamientos. Esto se refiere tanto a la necesidad de combinar diferentes fármacos durante la misma etapa como a la consecución de fármacos conforme vaya avanzando el proceso oncológico.
Esto es debido a que, en ocasiones, las células cancerosas pueden cambiar su mutación o presentar múltiples mutaciones de aquellas identificadas inicialmente. Normalmente se produce como una respuesta del cáncer a los tratamientos a los que está sometido. Esto puede significar la alteración del tratamiento a uno más específico contra las nuevas mutaciones.
A las etapas de consecución de tratamientos se las conoce como líneas y la primera de ellas se corresponde con aquellos tratamientos que recibe una persona paciente en el momento en el que es diagnosticada. Los tratamientos de primera línea suelen ser aquellas terapias dirigidas cuando se conocen los biomarcadores concretos del tumor, o la inmunoterapia, quimioterapia o una combinación de ambas cuando se trata de tumores con niveles altos de la proteína PD-L1.
Las líneas posteriores –segunda y tercera línea– dependerán de las características de la enfermedad, de los tratamientos de primera línea ya recibidos y de las mutaciones que el tumor posee, tanto las identificadas en el diagnóstico como las que han ido apareciendo. Para los tratamientos de tercera línea suele recurrirse a la quimioterapia.
Al igual que cada persona recibirá un tratamiento distinto y reaccionará de manera diferente a los tratamientos, las líneas de tratamientos también serán distintas para cada paciente.
En el caso del cáncer de pulmón de células pequeñas, se recurre a la quimioterapia como tratamiento único en la mayoría de las ocasiones. La radioterapia es fundamental en aquellos casos en los que la enfermedad está limitada al tórax.
Tratamientos actuales
Tratamientos actuales
Para conocer más sobre los medicamentos concretos que están actualmente vigentes en España, puedes encontrar los informes en la Agencia Española de Medicamentos y Productos Sanitarios o en el Centro de Información de Medicamentos de la AEMPS.
¿Qué son los cuidados paliativos?
¿Qué son los cuidados paliativos?
Gracias a los avances de la medicina y la investigación de las últimas décadas numerosas enfermedades se pueden cronificar pero, por desgracia, no siempre el control de la patología es posible. Asistimos entonces al proceso del final de la vida de la persona. En ambos casos, los cuidados paliativos nos ofrecen las herramientas de control integral para el manejo de la situación, tanto a nivel médico, como psicológico, social y espiritual.
La Organización Mundial de la Salud (OMS) define el cuidado paliativo como la prevención y el alivio del sufrimiento a través de la detección temprana y correcta evaluación, el tratamiento del dolor y otros problemas que pueden ser físicos, psicológicos o espirituales (1). A continuación vamos a analizar cada uno de estos conceptos:
Una detección temprana implica que la intervención se pueda llevar a cabo desde fases precoces de la enfermedad, siempre que la persona requiera un tratamiento para paliar el dolor u otros síntomas de difícil control. Es un error pensar que los cuidados paliativos son un recurso exclusivo para fases finales de enfermedad, y como dice A. Pacual (2), es importante que se pueda realizar una intervención basada en “necesidades” más que en un plazo concreto de supervivencia, tal y como queda recogido en la Estrategia en Cuidados Paliativos del Sistema Nacional de Salud (SNS).
Una correcta evaluación requiere de la presencia de un equipo interdisciplinar, o en su defecto, de la interacción de los diferentes equipos asistenciales que atienden a la persona enferma y a su familia y de su buena comunicación y derivación fluida, para cubrir las necesidades médicas, psicológicas y sociales; es decir, tal y como recoge la Estrategia del SNS, una “atención integral, organizada y coordinada”. Además, como ciudadanía seguimos participando de forma activa en los planes de la Administración para que este derecho de atención integral sea una realidad global.
Una atención integral también supone evaluar el proceso de adaptación de la familia y, sobre todo, de la persona cuidadora principal y dar respuesta a las necesidades familiares que puedan surgir. El núcleo familiar es el que cuida a la persona enferma las 24 horas y, por ello, también necesita y recibe cuidados.
¿Y a qué llamamos necesidades espirituales? Como recoge L. Galiana en su artículo (3), se considera la espiritualidad como “una dimensión básica inherente al ser humano, que puede ser un recurso para trascender el sufrimiento, y lleva a contemplar la enfermedad como un reto para descubrir la propia naturaleza espiritual y crecer como persona”. No hace referencia solo a creencias religiosas, sino a la capacidad de encontrar sentido a la vida, de sentir plenitud ante lo vivido, de sentirse en paz con uno mismo y con los demás. La enfermedad oncológica siempre coloca a la persona ante la realidad de la muerte y despierta esta dimensión de la espiritualidad, a veces dormida durante años; pero igual que somos seres sociales, también somos seres espirituales que nos planteamos preguntas sobre el por qué y para qué de la situación que se está viviendo.
Respecto al “tratamiento del dolor”, es importante incidir en que toda persona en cuidados paliativos que padece dolor requiere una atención, es decir, el dolor no es una queja, es una realidad. La percepción del dolor es algo subjetivo, cierto, pero no podemos minimizar una expresión de dolor. Debemos, eso sí, evaluarlo desde una mirada multifactorial, contemplando la realidad física y también la influencia de aspectos emocionales u otro tipo de preocupaciones (familiares, sociales, económicas, asuntos pendientes de resolución, etc).
Desde la dimensión psicológica se contempla lo que Cicely Sounders llamó “dolor total”, que implica la consideración y abordaje de aspectos relativos al momento vital, el significado e impacto de la enfermedad, estilo de afrontamiento, recursos espirituales, situación socioeconómica y la valoración de otros aspectos como la influencia de las actitudes, las creencias, la autoimagen, la personalidad, el estilo de comunicación de la familia y la etapa evolutiva del ciclo vital familiar (4).
La enfermedad oncológica a menudo conlleva cambios en la vida no solo de la persona, sino también de la familia, y es necesaria la revisión de todos estos aspectos multifactoriales para poder comprender y aceptar la forma de adaptación de la persona al proceso de la enfermedad.
Es importante eliminar el tabú de hablar de la muerte para poder reclamar unos cuidados de calidad, de manera consensuada con la familia y con el equipo médico, y poder plantear las voluntades anticipadas, transmitiendo a nuestros seres queridos valores y preferencias en torno a decisiones sobre los cuidados (5).
Los cuidados paliativos, como vemos, aportan a la persona enferma y a su familia un tratamiento global y, sobre todo, un cuidado, un espacio de escucha y un soporte emocional que les facilite transitar la enfermedad con mayor seguridad y confianza. Y este es el trabajo que ofrecemos desde la Asociación Carena CARENA (6): apoyo psicológico integral, en situaciones de enfermedad grave, en colaboración con algunos hospitales de la ciudad de Valencia y en Denia.
Referencias:
1- Organización Mundial de la Salud OMS
5- Inscripción en el Registro del Documento de Voluntades Anticipadas. Generalitat Valenciana.
6- Asociación Carena
Facebok: Carena Asociacion | Instagram: asociacioncarena | Twitter: @AsocCarena
